【產地國家】: 日本
【處方 藥】: 是
【所屬類別】: 90毫克/0.6毫升/瓶
【包裝規格】: 90毫克/0.6毫升/瓶
【計價單位】: 瓶
【生產廠家中文參考譯名】:
中外制藥
【生產廠家英文名】:
Chinese and foreign pharmaceutical
【該藥品相關信息網址】:
http://www.info.pmda.go.jp/go/pack/6343451A1025_1_01/
【原產地英文商品名】:
HEMLIBRA
【原產地英文藥品名】:
Emicizumab(Genetical Recombination)
【中文參考商品譯名】:
HEMLIBRA
【中文參考藥品譯名】:
重組艾米希組單抗
【簡介】:
部份中文HEMLIBRA處方資料(僅供參考)
英文名:Emicizumab(Genetical Recombination)
商標名:HEMLIBRA
中文名:重組艾米希組單抗
生產商:中外制藥
【藥品簡介】
抗血液凝固第IXa/X因子ヒト化二重特異性モノクローナル抗體血液凝固第VIII因子機能代替製剤
批準日期:2018年5月
商標名
HEMLIBRA
(Emicizumab(Genetical Recombination))(JAN)
【處理注意事項】
保存記錄由于該藥物不是特定生物來源的產品,而是血液制品替代藥物,當給予(處方)藥物時,藥物名稱及其序列號,給藥日期(處方),使用的患者姓名 ,地址等,并保存至少20年。
【批準條件】
1.制定藥品風險管理計劃并適當實施。
2.由于日語管理經驗非常有限,在制造和銷售期間累積了一定數量的案例數據之前,通過對所有案例進行使用結果調查 ,掌握使用該藥物的患者的背景信息,盡快收集該藥物的安全性和有效性數據,并采取必要措施正確使用該藥物。
【藥用藥理學】
1.該藥物通過等離子體共振方法在體外蛋白結合測定系統中與活性型凝血因子IX和凝血因子X結合,并在體外酶促反應測定系統中通過合成顯色底物法與活性酶型凝血測定系統結合。 因子IX促進血液凝固因子X的活化。
2.該試劑通過體外添加凝血因子VIII缺乏的含血漿抑制劑和不含抑制劑的凝血因子VIII缺乏血漿,顯示APTT縮短和凝血酶產生增加,推廣。
3.在通過給予抗凝血因子VIII抗體誘導血友病A的猴子中觀察到通過給予該藥物的出血傾向抑制作用和止血作用。
【適應癥】
抑制具有抗凝血因子VIII抑制劑的先天性凝血因子VIII缺乏患者的出血傾向
【用法與用量】
通常,每周4次,3mg / kg(體重),因為emicizumab(遺傳重組)皮下注射皮下四次,隨后每周一次以1.5mg / kg(體重)皮下施用,間隔一次。
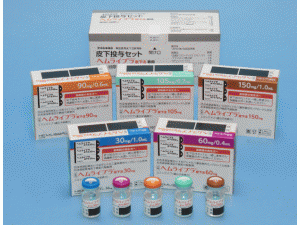
包裝
皮下注射
30mg:1.0mL×1小瓶
60mg:0.4mL×1小瓶
90mg:0.6mL×1小瓶
105mg:0.7mL×1小瓶
150mg:1.0 mL×1小瓶
制造供應商
中外制藥有限公司
完整說明書附件:http://www.info.pmda.go.jp/go/pack/6343451A1025_1_01/
(責任編輯:admin)
聯系祺昌
24小時服務熱線:(086)150 1799 1962 / (086)189 2841 1962