近日,美國Amgen公司的地舒單抗注射液(Denosumab Injection)在國內的第三個新增適應癥申請(相關受理號為JXSS19000009)進入行政審批階段,這意味著該藥有望在國內獲批第三個適應癥。據悉此次即將獲批的適應癥是: 多發性骨髓瘤和實體瘤骨轉移患者中骨相關事件的預防 。
據了解,增加適應癥是指在說明書種增加一個適應癥條款,或某活性成分獲批新的適應癥,不包括擴大適應人群的年齡范圍、擴大適應癥的嚴重程度,由二線藥物調整為一線藥物等。

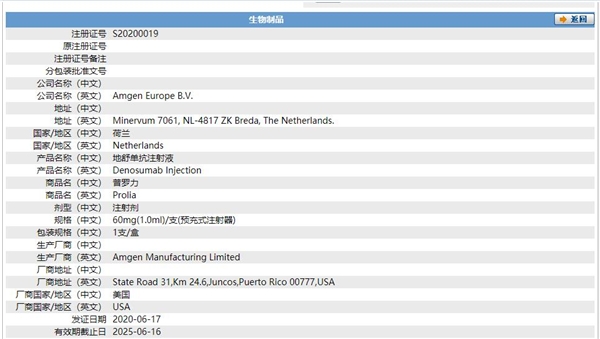
地舒單抗注射液(安加維®)(英文商品名 XGEVA®,通用名:地舒單抗注射液,Denosumab Injection),是一種人免疫球蛋白G2(IgG2)單克隆抗體,對RANKL具有高特異性和親和性。該藥通過與RANKL結合,阻止破骨細胞的RANK信號通路的激活,打破了癌癥骨轉移的"惡性循環",從而達到抑制腫瘤生長和減少骨質破壞的目的。該藥于 2019年5月被NMPA用于治療不可手術切除或者手術切除可能導致嚴重功能障礙的骨巨細胞瘤,包括成人和骨骼發育成熟(定義為至少1處成熟長骨且體重≥45 kg)的青少年患者,商品名為安加維。

2020年6月,地舒單抗又被NMPA批準用于骨折高風險的絕經后婦女的骨質疏松癥治療,商品名為普羅力,成為國內首個,也是目前唯一一個用于骨質疏松癥治療的抗 RANKL單抗類藥物。
骨轉移是晚期惡性腫瘤常見并發癥之一,特別是晚期乳腺癌、前列腺癌、肺癌等,平均每3個患者就會有一個發生骨轉移。晚期腫瘤骨轉移患者一旦發生病理學骨折、脊髓壓迫、高鈣血癥等骨相關事件,就會對患者的生活和生存造成極大的負面影響。目前國內預防和治療骨轉移相關事件的藥物主要是雙磷酸鹽類藥物,如唑來膦酸、伊班膦酸、帕米膦酸。
而地舒單抗在國外(英文商品名 XGEVA®,通用名:地諾單抗注射液,Denosumab Injection)已被批準用于預防晚期腫瘤骨轉移患者的骨相關事件。相較雙磷酸鹽類藥物,地諾單抗用于預防骨相關事件時如下優勢:
(1)不僅具有靶向性,而且還具有直接抗腫瘤作用;
(2)臨床療效優于雙磷酸鹽類藥物,且對雙磷酸鹽類藥物治療失敗的患者仍有效;
(3)安全性好,應用地舒單抗的患者更少出現腎毒性的副作用;
(4)使用方便,雙磷酸鹽類藥物需要靜脈注射,而地舒單抗為皮下注射,使用更方便。
期待地舒單抗用于預防骨相關事件的適應癥可以早日獲批。更為重要的是,相比國內的地舒單抗,進口地諾單抗價格反而可以便宜一大半,需要可聯系#香港濟民藥業#,長期現貨供應 ,專業冷鏈配送。
24小時服務熱線:(086)150 1799 1962 / (086)189 2841 1962
