OncoSec Medical是一家專注于開發基于DNA的瘤內腫瘤免疫療法的生物技術公司。近日,該公司公布了實驗性瘤內DNA腫瘤免疫療法ImmunoPulse IL-12兩項II期臨床研究(OMS-I100,OMS-I102)的更新數據。OMS-I100是一項單藥研究,在51例轉移性黑色素瘤患者中開展,研究中患者僅接受ImmunoPulse IL-12單藥治療。OMS-I102是一項組合研究,在22例轉移性黑色素瘤患者中開展,這些患者經基線生物標志物數據被預測為不會對抗PD-1療法產生治療反應,研究中患者接受ImmunoPulse IL-12治療的同時也接受默沙東PD-1免疫療法Keytruda(pembrolizumab,每3周一次)治療。
此次公布的數據證實,ImmunoPulse IL-12無論是單藥治療或是與Keytruda聯合用藥,均能觸發關鍵的免疫事件,驅動一種可導致“腫瘤發炎(inflamed tumor)”的細胞反應,將“冷的”腫瘤(“cold”tumors)轉變為“熱的”腫瘤(“hot”tumors),這種細胞反應在聯合Keytruda用藥時得到進一步的增強。
OMS-I100研究的關鍵結果:(1)采用修正的“皮膚”RECIST評價,最佳總緩解率為25-34.6%;(2)研究中,ImmunoPulse IL-12具有良好的安全性,未發生危及生命的或4級不良事件;(3)在接受90天為周期ImmunoPulse IL-12治療的患者(n=26)中,完全緩解率為19.2%(5/26),部分緩解率為15.4%(4/26),疾病穩定率為34.6%(9/26),總的疾病控制率為69.2%;(4)在接受6周為周期ImmunoPulse IL-12治療的患者中(n=20),完全緩解率為0%,部分緩解率為25%(5/20),疾病穩定率為40%(8/20),總的疾病控制率為65%。
IMS-I102研究的關鍵結果:(1)在治療24周期間,觀察到的最佳總緩解率(BORR)為50%(n=11/22),其中42.9%(9/21)達到了RECIST v1.1(實體腫瘤的療效評價標準1.1版)的BORR。(2)完全緩解率(CR)為41%(n=9/22),部分緩解率(PR)為9%(n=2/22),疾病穩定率(SD)為9%(n=2/22),總的疾病控制率為59%,其中38.1%(n=8/21)達到了RECIST v1.1的持續完全緩解。(3)研究數據表明,ImmunoPulse IL-12與Keytruda聯合用藥,能觸發一種協調的先天免疫和適應性免疫,提示ImmunoPulse IL-12與抗PD-1療法具有協同作用。
這2項研究的首席研究員、加利福尼亞大學(UCSF)副教授Alain Algazi博士表示,這些分析數據非常令人鼓舞,數據繼續證實ImmunoPulse IL-12能觸發免疫系統幫助提高患者對PD-1療法的治療反應。組合研究中,ImmunoPulse IL-12與Keytruda聯合用藥在被預測為抗PD-1無應答的患者群體中所取得的完全緩解率數據提供了令人信服的早期證據,即該組合可能為對PD-1免疫療法無應答患者群體帶來臨床意義的治療受益。
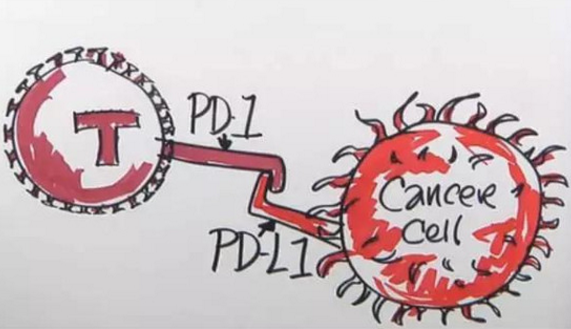
ImmunoPulse IL-12:將解決PD-1/PD-L1療法難治或無緩解患者群體中的顯著醫療需求
IL-12是一種體內自然產生的蛋白質,具有免疫刺激功能。pIL-12(一種可表達白細胞介素-12[IL-12]的質粒)是ImmunoPulse IL-12中的活性生物制劑,后者是一種潛在首創(first-in-class)的瘤內抗癌基因療法,通過瘤內注射及短脈沖電穿孔遞送至腫瘤微環境中,產生受控的、局部表達的IL-12,從而使免疫系統能夠靶向并攻擊腫瘤細胞。目前,ImmunoPulse IL-12正處于臨床開發,用于轉移性黑色素瘤和三陰性乳腺癌(TNBC)的治療。在I期和II期臨床研究中,其針對多種實體瘤具有良好的安全性,同時表現出明顯的抗腫瘤活性和系統性免疫應答。
今年5月,默沙東與OncoSec達成了一項臨床合作協議,啟動多中心IIb期注冊研究PISCES,該研究將在既往接受已上市抗PD-1療法(包括Keytruda和Opdivo)治療后病情進展的局部晚期或轉移性黑色素瘤(階段III或IV)患者中開展,評估ImmunoPulse IL-12與Keytruda聯合用藥的療效和安全性。雙方的合作將專注于對PD-1/PD-L1療法難治或無緩解的黑色素瘤患者群體中顯著未滿足的醫療需求。
(責任編輯:admin)
聯系祺昌
24小時服務熱線:(086)150 1799 1962 / (086)189 2841 1962